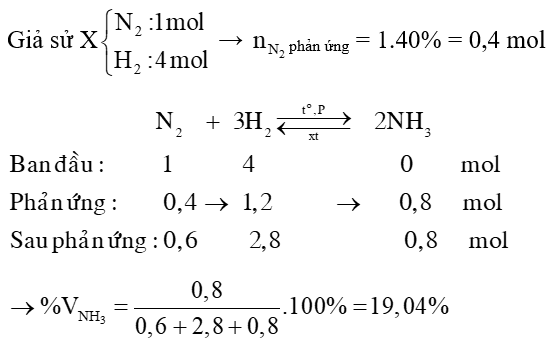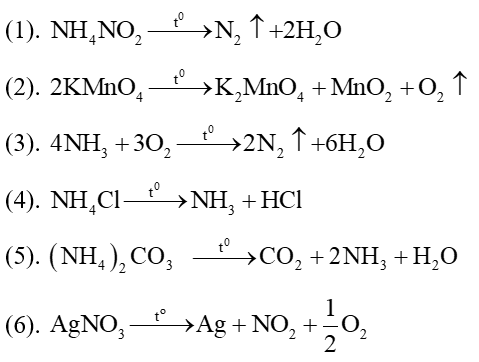Tailieumoi.vn xin giới thiệu phương trình 4NH3 + 3O2 → 2N2 + 6H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Nito. Mời các bạn đón xem:
Phương trình 4NH3 + 3O2 → 2N2 + 6H2O
1. Phương trình phản ứng hóa học
4NH3 + 3O2 →to 2N2 + 6H2O
2. Hiện tượng nhận biết phản ứng
Có khí thoát ra
3. Điều kiện phản ứng
- Nhiệt độ
4. Tính chất hoá học
- Là chất khí tan rất nhiều trong nước.
Tính bazo yếu:
+ Phản ứng với nước: NH3 + H2O ⇋ NH4+ + OH-.
+ Phản ứng với axit tạo muối amoni: NH3 + HCl → NH4Cl (amoni clorua).
+ Phản ứng với dung dịch muối:
AlCl3 + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4Cl
Al3+ + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4+
Tính khử:
Phản ứng được với oxi, clo và khử một số oxit kim loại.
Khả năng tạo phức chất tan:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
AgCl + 2NH3 → [Ag(NH3)2]Cl
5. Cách tiến hành thí nghiệm
Đốt cháy khí NH3 trong khí O2.
6. Bạn có biết
- Sản xuất axit nitric, các loại phân đạm như urê (NH2)2CO; NH4NO3; (NH4)2SO4; …
- Điều chế hiđrazin (N2H4) làm nhiên liệu cho tên lửa.
- Amoni lỏng dùng làm chất gây lạnh trong thiết bị lạnh.
7. Bài tập liên quan
Câu 1: Oxi hoá NH3 bằng CrO3 sinh ra N2, H2O và Cr2O3. Số phân tử NH3 tác dụng với một phân tử CrO3 là
A. 3.
B. 1.
C. 4.
D. 2.
Hướng dẫn giải:
Đáp án B
2NH3 + 2CrO3 →to N2 + 3H2O + Cr2O3
→ 1 phân tử NH3 phản ứng với 1 phân tử CrO3.
Câu 2: Cho cân bằng hóa học (trong bình kín) sau:
N2(khí) + 3H2(khí) ⇄ 2NH3 ; ∆H = -92kJ/mol
Trong các yếu tố:
(1) Thêm một lượng N2 hoặc H2.
(2) Thêm một lượng NH3.
(3) Tăng nhiệt độ của phản ứng.
(4) Tăng áp suất của phản ứng.
(5) Dùng thêm chất xúc tác.
Có bao nhiêu yếu tố làm cho cân bằng dịch chuyển theo chiều thuận ?
A. 3
B. 4
C. 5
D. 2
Hướng dẫn giải:
Đáp án D
Các yếu tố: 1, 4.
+ (1): Thêm lượng N2 hoặc H2 → cân bằng dịch chuyển theo chiều làm giảm N2/ H2(chiều thuận)
+ (2): Thêm NH3→ cân bằng dịch chuyển theo chiều làm giảm NH3 (chiều nghịch)
+ (3): ∆H = -92 < 0 → phản ứng thuận là tỏa nhiệt → tăng nhiệt độ làm cân bằng chuyển dịch theo chiều thu nhiệt (chiều nghịch)
+ (4): Tăng áp suất của phản ứng → cân bằng dịch chuyển theo chiều giảm áp suất (chiều thuận)
+ (5): Chất xúc tác không làm ảnh hưởng đến cân bằng hóa học
Câu 3: Người ta điều chế phân urê bằng cách cho NH3 tác dụng với chất nào (điều kiện thích hợp):
A. CO2
B. CO
C. HCl
D. Cl2
Hướng dẫn giải:
Đáp án A
Phân urê là (NH2)CO.
Điều chế:
CO2 + 2NH3 →to,P (NH2)2CO + H2O
Câu 4:Hợp chất nào sau đây nitơ có số oxi hoá là -3:
A. NO.
B. N2O.
C. HNO3.
D. NH4Cl.
Hướng dẫn giải:
Đáp án D
N+2O,N+12O,HN+5O3,N−3H4Cl
Câu 5:Hỗn hợp X gồm N2 và H2 với tỉ lệ mol là 1:4. Nung hỗn hợp X ở điều kiện thích hợp để phản ứng xảy ra. Biết hiệu suất phản ứng là 40%. Phần trăm theo thể tích của amoniac (NH3) trong hỗn hợp thu được sau phản ứng là:
A. 16,04%.
B. 17,04%.
C. 18,04%.
D. 19,04%.
Hướng dẫn giải:
Đáp án D
Dễ thấy hiệu suất tính theo N2
Câu 6: Chất nào sau đây có thể làm khô khí NH3 có lẫn hơi nước ?
A. P2O5.
B. H2SO4 đặc.
C. CuO bột.
D. NaOH rắn.
Hướng dẫn giải:
Đáp án D
Chất dùng làm khô khí NH3 có lẫn hơi nước phải là chất có đặc tính hút nước và không phản ứng với NH3.
→ Dùng NaOH rắn để làm khô khí.
Câu 7: Muối được làm bột nở trong thực phẩm là
A. (NH4)2CO3.
B. Na2CO3.
C. NH4HCO3.
D. NH4Cl.
Hướng dẫn giải:
Đáp án C
Người ta dùng muối NH4HCO3 làm bột nở trong thực phẩm.
Câu 8:Có ba dung dịch mất nhãn: NaCl; NH4Cl; NaNO3. Dãy hoá chất nào sau đây có thể phân biệt được ba dung dịch :
A. Phenol phtalein và NaOH.
B. Cu và HCl.
C. Phenol phtalein; Cu và H2SO4 loãng .
D. Quỳ tím và dung dịch AgNO3.
Hướng dẫn giải:
Đáp án D
- Khi cho quỳ tím vào 3 mẫu thử thì chỉ có NH4Cl làm quỳ tím hóa đỏ. Do hiện tượng thủy phân của NH4Cl: NH4++H2O⇄NH3+ H3O+
- Cho AgNO3 vào 2 dung dịch còn lại thì NaCl tạo kết tủa trắng.
AgNO3 + NaCl → AgCl↓ + NaNO3
Câu 9:Hỗn hợp X gồm N2 và H2 có tỉ khối so với hiđro là 6,2. Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y. Tỉ khối của hỗn hợp khí Y hiđro là:
A. 14,76.
B. 18,23.
C. 7,38.
D. 13,48.
Hướng dẫn giải:
Đáp án C
N2 + 3H2 ⇄xtto,P 2NH3
Áp dụng sơ đồ đường chéo cho hỗn hợp N2 và H2 ta có: nN2nH2=23
=> H2 thiếu, hiệu suất phản ứng tính theo H2.
Chọn
nH2pư= 3.40% = 1,2 mol
→ nN2pư = 0,4 mol và nNH3sinh ra =0,8 mol.
ny = nx - 0,8 = 2 + 3 - 0,8 = 4,2 mol
Bảo toàn khối lượng:
→ M¯YM¯X=nXnY → M¯Y=5.6,2.24,2 = 14,76
→ Tỉ khối của Y với H2 là 7,38.
Câu 10: Cho các thí nghiệm sau :
(1). NH4NO2 →to
(2). KMnO4 →to
(3). NH3 + O2 →to
(4). NH4Cl →to
(5). (NH4)2CO3 →to
(6). AgNO3 →to
Số thí nghiệm tạo ra đơn chất là :
A. 6
B. 5
C. 4
D. 3
Hướng dẫn giải:
Đáp ánC
Số thí nghiệm tạo ra đơn chất là (1), (2), (3) và (6).
8. Một số phương trình phản ứng hoá học khác của Nito và hợp chất:
8NH3 + 3Cl2 → N2 + 6NH4Cl
NH3 (k) + HCl (k) → NH4Cl (r)
3NH3 + AlCl3 + 3H2O → Al(OH)3↓ + 3NH4Cl
NH4Cl + AgNO3 → AgCl↓ + NH4NO3
NH4Cl + NaOH → NaCl + NH3↑ + H2O
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 ↑ + 2H2O
2NH4Cl + Ba(OH)2 → BaCl2 + 2NH3 ↑+ 2H2O